Szczepionki na Covid-19. Skąd te wszystkie problemy UE?

Nie ma chyba obecnie gorętszego tematu w Polsce niż szczepionki na Covid-19. 25 stycznia zaczęły się masowe szczepienia. Ale szybko okazało się, że ruszą z opóźnieniem m, bo nie zaszczepiła się jeszcze nawet grupa „0” . Po prostu nie ma czym szczepić. Szczepionek brak w całej Unii Europejskiej. Poniżej postaram się pokazać Ci w prosty sposób dlaczego i na co realnie możemy liczyć w najbliższej przyszłości.
Szczepionki na Covid-19: strategia Unii
Wbrew pozorom o tym ile i kiedy dotrą do nas szczepionki na Covid-19, nie decyduje polski rząd lecz umowy zawierane z poszczególnymi producentami szczepionek przez Unię Europejską. A ściślej mówiąc przez Komisję Europejską, która Unię reprezentuje.
17 czerwca 2020 r. Unia ogłosiła „Strategię Szczepień UE”. Zasady są proste: Unia postawiła na różnorodność typów i źródeł szczepionki. Czyli kupujemy od kilku różnych producentów, różne typy szczepionek.
Poza tym kupujemy wspólnie, jako Unia Europejska, a Komisja negocjuje warunki zakupu w imieniu państw członkowskich.
Dlatego zakup i dostawa szczepionek na Covid-19 do Polski odbywa się na podstawie tzw. umów zakupu z wyprzedzeniem (ang. Advance Purchase Agreement – APA).
Nasz kraj przystąpił do unijnego porozumienia dotyczącego opracowania, produkcji, priorytetowych opcji zakupu oraz dostaw szczepionki na COVID-19 do państw członkowskich Unii Europejskiej na postawie uchwały Rady Ministrów nr 114/2020 Rady Ministrów z dnia 10 sierpnia 2020 r. Do wykonywania porozumienia Polska-Unia w sprawie szczepionek został upoważniony nasz Minister Zdrowia.
Z kim Unia zawarła już umowę, z kim nie i na zakup ilu dawek szczepionek na koronawirusa dowiesz się z mojej tabelki poniżej:
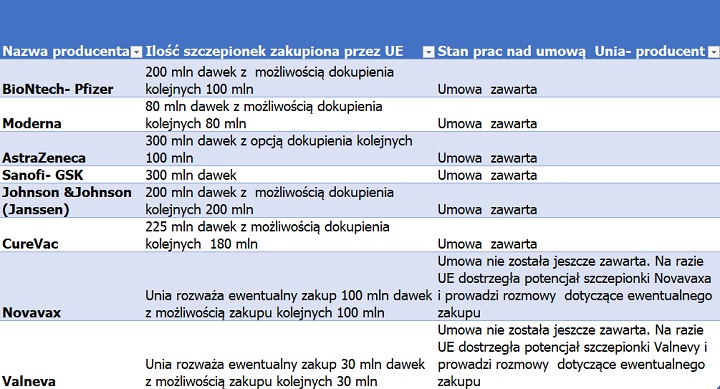
Wszystkie dane pochodzą ze strony Europejskiej Agencji Leków (ang. European Medicines Agency (EMA))
Tylko 3 z 8 producentów, którzy mają dostarczać szczepionki do Unii w ogóle jakąś szczepionkę ma
Przyznasz chyba, że na pierwszy rzut oka unijna strategia szczepień wygląda rozsądnie. UE zapewnia swoim obywatelom wystraczającą ilość szczepionek i to od różnych producentów. Ma to sens. Jeden czy dwóch może nawalić (chociażby nieprzewidziane awarie linii produkcyjnych), ale wszyscy na raz raczej nie. To samo ze skutecznością szczepionki. Gdyby jeden typ nie zadziałał, to zawsze mamy w odwodzie produkt innego producenta.
Jest tylko jedno „ale” a w zasadzie kilka.
Po pierwsze, kiedy powstaje ten tekst, tylko 3 z 8 wybranych przez Unię producentów szczepionki już ją „ma”. Czyli zakończyło wystarczającą ilość badań klinicznych I, II i III fazy (o tym czym są fazy badań klinczych pisałam już wcześniej), żeby stwierdzić, że preparat jest skuteczny i jednocześnie bezpieczny dla ludzi. Ci trzej producenci to BioNTech-Pfizer, Moderna i AstraZeneca.
Pozostałych 5 producentów to: Sanofi-GSK, Johnson&Johnson, CureVac, Novavax i Valvena. Ich szczepionki na Covid-19 albo nie weszły jeszcze w III, ostatnią fazę, badań albo wyniki badań III fazy są złe. W tę ostatnią pułapkę wpadł na przykład francuski koncern Sanofi-Aventis, który prowadzi badania nad szczepionką we współpracy z brytyjskim GSK (GlaxoSmith&Kline). Badanie III fazy wykazały, że szczepionka Sanofi-GSK jest nieskuteczna w walce z koronawirusem u osób powyżej 50 roku życia. Będzie powtórka badań, tym razem ze zmienionym składem szczepionki, a to oznacza opóźnienia. Sanof-GSK uznało, że na tyle duże, iż jest gotowe udostępnić swoje francuskie linie produkcyjne do produkcji szczepionek BioNTech-Pfizer lub AstraZeneca. Rozmowy już podobno trwają.
Nie trzeba geniusza, żeby stwierdzić, że w tej sytuacji z tą różnorodnością źródeł dostaw i rodzajów szczepionek, to raczej kiepsko. Bo Unia ma tej chwili tylko 3 producentów, którzy są w stanie cokolwiek dostarczyć.

…A Ci co mają już zapowiedzieli ograniczenie dostaw
Po drugie, na ograniczonym wyborze producentów szczepionek kłopoty UE się nie kończą. Dziwnym zbiegiem okoliczności i BioNTech-Pfizer i Moderna i AstraZeneca ogłosiły, że nie dadzą rady dostarczyć tylku dawek szczepionki na ile się zgodzili w umowach z UE.
Cała trójka tłumaczy to trudnościami produkcyjno-logistycznymi. I tak BioNTech-Pfizer zapowiedział już z początkiem stycznia, że ogranicza liczbę dostaw, bo musi zmodernizować linię produkcyjną w Belgii. Z kolei amerykańska Moderna już z końcem grudnia poinformowała, że ma potężne kłopoty logistyczne i produkcyjne już na poziomie dostaw w Stanach Zjednoczonych. Pamiętajmy, że Moderna to mała firma. Zatrudnia zaledwie ok. 900 osób na świecie. Wreszcie AstraZeneca poinformowała w w połowie stycznia, że ma problemy z linią produkcyjną w Belgii, a to oznacza, że Unia dostanie o 60% mniej szczepionek niż zakontraktowała. Co prawda koncern uważa, że zmniejszenie dostaw potrwa tylko w I kwartale 2021, ale nie wiadomo czy przewidywania się sprawdzą.
Efekt jest taki, że umowy o dostawę szczepionek są zawarte, ale żaden z producentów, nie zamierza się z nich wywiązać. Przynajmniej na razie. Wszyscy trzej tłumaczą się nieprzewidzianymi problemami logistyczno-produkcyjnymi. I oczywiście twierdzą, że nie naruszyli umów zawartych z UE, ale to już jest materiał na inny wpis.
Szczepionki na Covid-19 mają tylko warunkowe dopuszczenia do obrotu w UE
Po trzecie, nie do końca wiadomo jaką odporność na koronawirusa dają szczepionki i jak długo ta odporność potrwa. Oczywiście producenci podali swoje szacunki, ale prawda jest taka, że tego nie wie nikt. Poza tym wszystkie szczepionki na Covid-19 zostały w Unii tylko warunkowo dopuszczone do obrotu. W praktyce oznacza to, że Europejska Agencja Leków (EMA) zarekomendowała dopuszczenie szczepionek do użycia opierając się na niepełnych danych klinicznych. Spokojnie, to nic złego. Po prostu konieczność. Tylko procedura warunkowego dopuszczenia leku lub szczepionki do obrotu umożliwia przyspieszenie wydania pozwolenia na ich użycie we wszystkich krajach Unii. Gdyby EMA miała oceniać wnioski o „stałe” a nie „warunkowe” pozwolenie, to jeszcze długooo byśmy na jakąkolwiek szczepionkę poczekali.
W skocie, procedura warunkowego dopuszczenia do obrotu oznacza, że EMA ocenia na bieżąco dane z badań klinicznych przesłanych przez producenta. Robi to w ramach tzw. „przeglądów etapowych”. Jeśli dane są zadowalające, producent leku/szczepionki składa wniosek o warunkowe dopuszczenie produktu do obrotu w Unii. Jeśli EMA zarekomenduje wniosek pozytywnie, zatwierdza go Komisja Europejska (KE). Wydanie warunkowego pozwolenia oznacza, że nie zostało dane raz na zawsze, a producent musi dosłać EMie dodakowe dane kliniczne umożliwiające pełną ocenę już po wydaniu pozwolenia przez KE.
Przy czym nawet ta przyspieszona i skrótowa ocena wyników badań klinicznych jest dokładna. Nie ma możliwości, żeby EMA zarekomendowała warunkowe pozwolenie na dopuszczenie do obrotu szczepionki, która nie daje ochrony przed wirusem. Albo stwarza zagrożenie dla ludzkiego życia i zdrowia.
I tak ocenę skuteczności EMA częściowo „oblała” szczepionka Astry. EMA stwierdziła, że na podstawie dostarczonych przez firmę danych klinicznych nie rekomenduje użycia szczepionki u osób powyżej 55 roku życia.
Jak widzisz jest w tej szczepionkowo- unijnej układance bardzo dużo elementów. Często nieprzewidzianych. Dla lepszego rozeznania, poniżej wklejam gustowne tabelki z krótką informacją na temat pozwoleń oraz problemami ze szczepionką. A wszystko z podziałem na poszczególnych producentów. Dane zebrałam głównie z oficjalnej strony EMA.
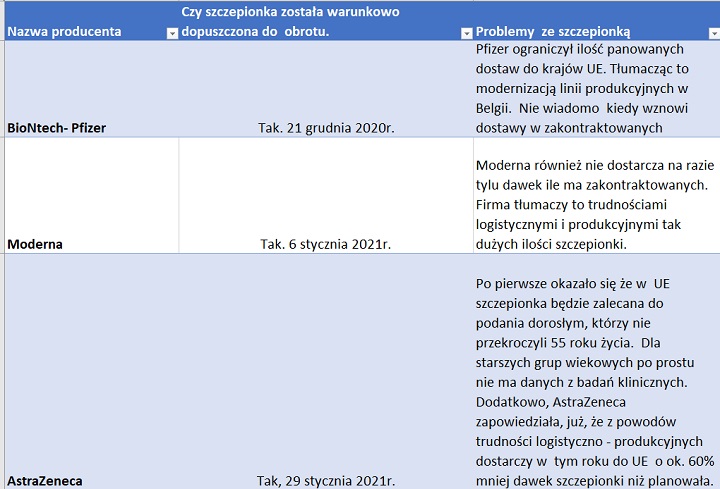

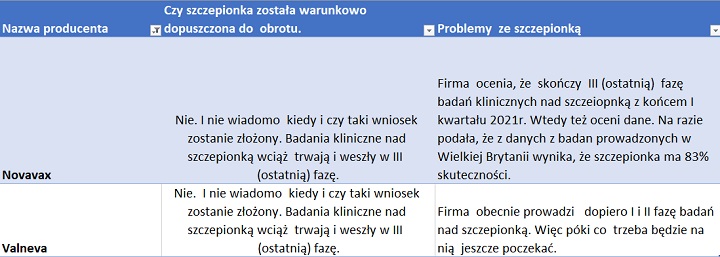
Pozdrawiam, Prawstoria




